A Agência Nacional de Vigilância Sanitária (Anvisa) recebeu o pedido de uso emergencial da CoronaVac, vacina contra a Covid-19 produzida pelo laboratório

Redação Publicado em 09/01/2021, às 00h00 - Atualizado às 14h38
A Agência Nacional de Vigilância Sanitária (Anvisa) recebeu o pedido de uso emergencial da CoronaVac, vacina contra a Covid-19 produzida pelo laboratório chinês Sinovac em parceria com o Instituto Butantan, na manhã desta sexta-feira (8). A agência pretende fazer a análise do uso emergencial em até 10 dias.
De acordo com o Butantan, o pedido de uso emergencial foi para as 6 milhões de doses que chegaram prontas da China e que fará um novo pedido para as doses envasadas no instituto em São Paulo. A solicitação foi feita durante uma reunião virtual, por causa da pandemia, às 9h34, segundo o Instituto Butantan. A Anvisa diz que já iniciou a triagem da documentação entregue.
“As primeiras 24h serão utilizadas para fazer uma triagem do processo e checar se todos os documentos necessários estão disponíveis. Se houver informação importante faltando, a Anvisa pode pausar o prazo e solicitar as informações adicionais ao laboratório”, afirmou a Anvisa, em nota.

Anvisa recebe pedido de uso emergencial do Butantan
A agência diz que a análise do pedido de uso emergencial é feita por uma equipe multidisciplinar, e envolve especialista das áreas de registro, monitoramento e inspeção.
O resultado final do estudo sobre a eficácia é a última etapa necessária para que a Anvisa analise o pedido de autorização de uso da vacina na população brasileira.
Caso a agência de vigilância identifique a pendência de alguma informação na documentação enviada, o prazo de análise pode ser superior aos 10 dias. “A meta da Anvisa é fazer a análise do uso emergencial em até 10 dias, descontando eventual tempo que o processo possa ficar pendente de informações , a serem apresentadas pelo laboratório”, diz em nota.

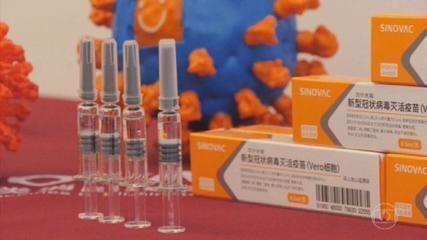
Caixa da Coronavac, vacina contra a Covid-19, em frente à sede do Instituto Butantan em São Paulo. — Foto: Aloisio Mauricio/Estadão Conteúdo
A Anvisa afirmou ainda que “atua, conforme os procedimentos científicos e regulatórios, os quais devem ser seguidos por aqueles que buscam o a autorização de vacinas para serem utilizadas na população brasileira.”
De acordo com o governo de São Paulo, a CoronaVac teve eficácia de 78% para casos leves na terceira fase de testes com cerca de 13 mil voluntários no Brasil. Para redução de casos graves e moderados, o governo anunciou índice de eficácia de 100%, ou seja, não houve casos graves (incluindo mortes) e moderados entre os vacinados.
No entanto, não foi divulgada a taxa de eficácia global, ou seja, não foi informado quantos voluntários que tomaram a vacina foram contaminados pela Covid-19 e nem quantos ficaram doentes após tomarem o placebo.
O governador João Doria (PSDB) chegou a afirmar que o pedido de registro emergencial já havia sido feito na quinta (7) durante coletiva de imprensa, mas depois a informação foi corrigida.
CoronaVac tem eficácia de 78% em testes feitos no Brasil, diz governo de SP
Segundo Dimas Covas, diretor do Instituto Butantan, o pedido de registro definitivo da vacina será feito posteriormente pelo laboratório chinês Sinovac, mas não informou a data exata.
“O pedido de registro da vacina será feito pela Sinovac. A Sinovac recolhe os dados dos estudos da vacina e é ela que submete o pedido oficialmente lá, na NMPA, que é a Anvisa chinesa, e imediatamente o mesmo pedido se estende ao Brasil e a outros países”, afirmou nesta quinta (7).
Segundo a Anvisa, o prazo para a análise do registro definitivo é feita em até 60 dias.
Em meados de dezembro, a Diretoria Colegiada da Anvisa aprovou as regras para a autorização temporária de uso emergencial, em caráter experimental, de vacinas contra a Covid-19.
Os principais pontos do uso emergencial das vacinas são seguintes:
A concessão estabelecida pela Anvisa segue o modelo de autorizações emergenciais adotadas em outros países, como Reino Unido, Estados Unidos e Canadá, e vale apenas para o período de pandemia e até a vacina receber o registro definitivo.

Entenda cada fase dos testes para vacinas
O governo de São Paulo espera que o uso emergencial seja autorizado pela agência até o dia 25 de janeiro, data estipulada no plano estadual de imunização para início da vacinação de 9 milhões de pessoas dos grupos prioritários.
Caso a vacina seja aprovada, profissionais da saúde, indígenas e quilombolas devem receber as primeiras doses, seguidos por idosos com mais de 60 anos.
Até esta quarta-feira (6), a Anvisa não havia recebido nenhum pedido para uso emergencial ou registro definitivo das outras vacinas que estão sendo testadas no Brasil. Dados complementares da fase 3 do imunizante desenvolvido pelo laboratório AstraZeneca e pela Universidade de Oxford foram recebidos, mas ainda sem o pedido de autorização.
Após apresentar parte dos dados de eficácia da vacina, o Butantan confirmou que assinou um contrato com o Ministério da Saúde para a aquisição de doses da CoronaVac, na noite de quinta-feira (7).
O documento prevê o fornecimento de 46 milhões de doses, em quatro entregas até o dia 30 de abril. Há ainda a possibilidade de o órgão federal adquirir do instituto outras 54 milhões de doses, totalizando 100 milhões.
Cada dose da vacina custará R$ 58,20 e o valor total do contrato é de R$ 2,6 bilhões.
O pagamento somente será realizado após a obtenção do registro ou autorização para uso emergencial junto à Agência Nacional de Vigilância Sanitária (Anvisa).
O contrato também prevê que o Ministério da Saúde “terá o direito de exclusividade na aquisição de doses da vacina”, podendo autorizar “em caráter excepcional a comercialização” para terceiros. Para isso, deverá ser “notificada formalmente sobre a intenção de venda com antecedência mínima de 20 dias.”
Como já foi dito, a utilização de uma vacina contra a Covid-19 no Brasil depende da aprovação pela Anvisa. A permissão pode ser conseguida, basicamente, por dois caminhos. O primeiro está diretamente ligado aos dois tipos de registro (tradicional ou emergencial), explicado acima, e a segunda possibilidade é baseada na chamada “Lei Covid” aprovada na Câmara dos Deputados, que libera o uso se o imunizante tiver aval expedido por uma agência do exterior, independentemente de registro pela Anvisa.
O acordo do Governo de São Paulo com a Sinovac prevê a compra de 46 milhões de doses, sendo 6 milhões já prontas e 40 milhões que serão processadas no Brasil a partir de matéria-prima chinesa.
No total, o governo de São Paulo recebeu até agora da China o equivalente a 10,8 milhões de doses da CoronaVac, considerando os lotes de vacina já pronta para aplicação e os de insumos que serão envasados pelo Instituto Butantan. Segundo o governo, mais 35 milhões de doses devem ser recebidas até fevereiro.
No dia 9 de dezembro, o Instituto Butantan começou o processo de envase da vacina a partir da matéria-prima importada da China. A processo é feito na fábrica do Butantan, que tem 1.880 metros quadrados, e contará com o reforço de 120 novos profissionais, além dos 245 que normalmente atuam no instituto.
Uma nova fábrica está sendo construída pelo Butantan para produção da vacina em território nacional. A previsão é que, quando pronta, ela seja capaz de produzir até 100 milhões de doses da CoronaVac por ano.
No fim de dezembro, a Anvisa publicou a certificação de Boas Práticas de Fabricação para a fábrica da CoronaVac na China. A conclusão foi feita pela equipe da Anvisa que viajou ao país para inspecionar a produção da farmacêutica Sinovac. O certificado tem validade de dois anos e é um do pré-requisitos tanto para o processo de registro da vacina no Brasil, quanto para o pedido de autorização para uso emergencial.
O estudo conclusivo mede a taxa de eficácia do imunizante comparando quantos casos confirmados ocorreram nos voluntários que receberam placebo e quantos naqueles que tomaram a vacina. A taxa mínima de eficácia recomendada pela Anvisa é de 50%.
No final do ano passado, a Turquia informou publicamente ter chegado ao percentual de 91,25% de eficácia da CoronaVac em testes preliminares feitos com 1,3 mil voluntários.
.
.
.
G1 – Globo.
Leia também

Indicado por Orlando Morando à Faculdade de Direito é alvo do Gaeco por corrupção e lavagem de dinheiro

Enfermeira é morta a tiros pelo ex-namorado na Zona Sul de SP

EXPLÍCITO: MC Mirella apela com vídeo de sexo para promover OnlyFans; assista

VÍDEO: Homem tenta estuprar nutricionista dentro de apartamento na Grande São Paulo

Youtuber Vitória Mineblox acusa pai de violência doméstica e denuncia suposto favorecimento do Conselho Tutelar de Tianguá

Quem defende o cidadão endividado?

Caso Henry: Monique Medeiros deixa a prisão, mas não foi absolvida; entenda o que decidiu a Justiça

Neymar fica fora de amistoso da Seleção contra o Egito

Uber anuncia demissões e acelera reestruturação em meio à corrida por IA

Lula ameaça retaliar EUA após nova ofensiva tarifária contra o Brasil