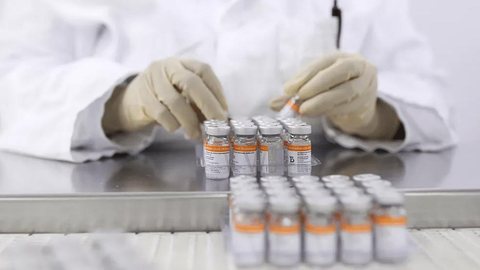
O Instituto Butantan, de São Paulo, entregou nesta sexta-feira (30) o estudo de imunogenicidade da vacina CoronaVac à Agência Nacional de Vigilância Sanitária
Redação Publicado em 01/05/2021, às 00h00 - Atualizado às 11h50
O Instituto Butantan, de São Paulo, entregou nesta sexta-feira (30) o estudo de imunogenicidade da vacina CoronaVac à Agência Nacional de Vigilância Sanitária (Anvisa). O documento atesta a capacidade da estimular o sistema imunológico a produzir anticorpos e é necessário para o registro provisório da CoronaVac na agência.
A entrega do documento estava prevista inicialmente 28 de fevereiro, mas, a pedido do Butantan, a Anvisa prorrogou o prazo para esta sexta. Esses estudos, segundo a agência, servirão para complementar o conhecimento brasileiro sobre imunidade conferida aos voluntários que receberam a vacina na etapa clínica dos ensaios na fase 3.
A falta de dados detalhados sobre a imunogenicidade da CoronaVac havia sido destacada pelo gerente de medicamentos e produtos biológicos da Anvisa, Gustavo Mendes, durante a reunião da agência que concedeu o uso emergencial da vacina, em 17 de janeiro.
Na ocasião, a Anvisa afirmou que não foram apresentados os resultados da avaliação de imunogenicidade ao longo do tempo para esse estudo, de acordo com o que era esperado e definido no protocolo aprovado para esse estudo clínico. A agência destacou ainda que “o único resultado apresentado não foi considerado adequado para avaliação e conclusão de imunogenicidade”.
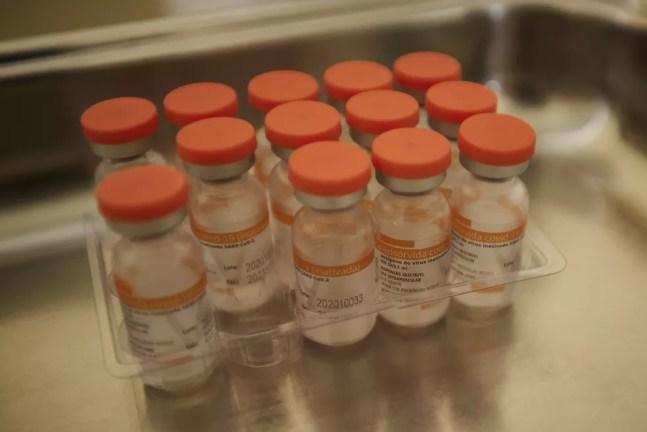
Doses da CoronaVac, vacina contra a Covid-19 produzida pela Sinovac em parceria com o Instituto Butantan. — Foto: IGOR DO VALE/ESTADÃO CONTEÚDO
Mesmo assim, a Anvisa garantiu que a vacina era segura, e deu um prazo de até 28 de fevereiro para que o Instituto Butantan apresentasse mais informações sobre a metodologia dos estudos.
Segundo o termo de compromisso, o Butantan precisa apresentar os resultados de como a produção de anticorpos ocorreu no grupo que tomou a vacina e no grupo que tomou placebo, em diferentes faixas etárias.
O registro definitivo das vacinas, quando aprovado, é válido por 10 anos. Mas, segundo o Instituto Butantan, o registro pleiteado será provisório, não definitivo, porque a vacina precisa ser acompanhada até o final dos estudos clínicos e também na pós-vacinação.
Para pedir o registro, o fabricante precisa apresentar dados completos sobre segurança, eficácia e qualidade, prazo de validade da vacina, definição dos grupos que podem tomar o imunizante, além do plano de monitoramento pós-vacinação e redução de riscos.
A pandemia da Covid-19 fez com que a Anvisa, de forma inédita, concedesse o uso emergencial para uma vacina, considerada experimental, que precisa de acompanhamento durante a aplicação e tem grupos específicos para receberem as doses. Com o registro, isso muda, e a vacinação pode ser feita em massa.
Além disso, o imunizante deixa de ser exclusivo do Sistema Único de Saúde (SUS) e pode ser comercializado à iniciativa privada. O valor da vacina é definido pela Câmara de Regulação do Mercado de Medicamentos (CMED), órgão interministerial presidido pelo Ministério da Saúde.
A empresa responsável pela vacina, com o registro, também tem os trâmites mais facilitados para a importação do imunizante na forma acabada e dos insumos usados na produção.
.
.
.
Fonte: Ge – Globo Esporte.
Leia também

Preocupação com sequestro leva pai a descobrir filho em lugar inimaginável

Ex-executivo processa companhia por causa de Cheetos picante; entenda o caso

Suposto vídeo de Mel Maia fazendo sexo com traficante cai na rede e atriz se manifesta

ONLYFANS - 7 famosas que entraram na rede de conteúdo adulto para ganhar dinheiro!

Polícia investiga suspeita de estupro em hospital particular

Ex-executivo processa companhia por causa de Cheetos picante; entenda o caso

Filipe Toledo é eliminado nas oitavas de final das Olimpíadas de Paris

Dívida pública avança para 77,8% do PIB

Estrangeiro é preso ao tentar transportar cocaína escondida em lugar peculiar; confira

Pai questiona valor da vida após filho ser atropelado por motorista de Porsche